干细胞治疗眼病的技术开发与临床研究进展

干细胞技术作为再生医学的核心,在眼科疾病治疗领域展现出前所未有的潜力。随着基础研究的深入和技术的不断迭代,干细胞治疗多种致盲性眼病已经从实验室研究逐步走向临床探索,为无数视力受损患者带来了新的希望。
一、干细胞治疗的主要技术路径与发展
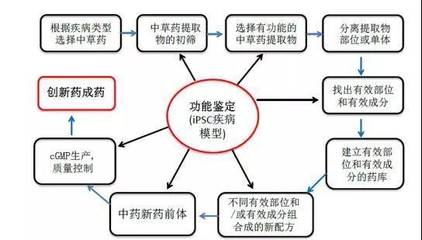
目前应用于眼病治疗的干细胞主要包括胚胎干细胞、诱导多能干细胞和成体干细胞(如间充质干细胞、角膜缘干细胞等)。技术开发的核心方向集中在几个关键环节:
- 细胞来源与定向分化:研究者已成功将干细胞定向分化为视网膜色素上皮细胞、光感受器前体细胞、角膜上皮细胞等特定眼组织细胞。特别是iPSC技术的成熟,实现了患者自体细胞的“重编程”,避免了免疫排斥和伦理争议。
- 递送技术与载体材料:开发了微创玻璃体腔注射、视网膜下腔注射以及生物材料支架(如水凝胶、纳米纤维膜)辅助移植等多种递送策略,旨在提高细胞存活率、整合精度与功能恢复。
- 质量控制与标准化:建立严格的细胞系鉴定、纯度检测、致瘤性评估及生产工艺标准,是技术向临床应用转化的基石。
二、临床研究进展与挑战
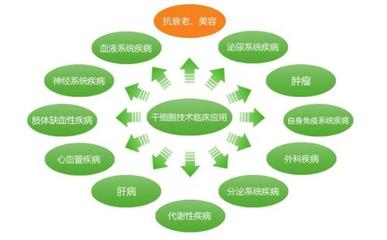
在疾病应用层面,干细胞治疗已针对多种眼病展开临床试验,并取得阶段性成果:
- 年龄相关性黄斑变性:多项I/II期临床试验表明,由ESC或iPSC分化而来的RPE细胞移植,能够稳定甚至部分改善晚期AMD患者的视力,且安全性在可控范围内。
- 视网膜色素变性:将光感受器前体细胞移植至视网膜下腔,在动物模型中显示出与宿主视网膜的结构整合及部分视觉功能恢复,早期人体试验正在进行中。
- 角膜疾病:利用角膜缘干细胞或口腔黏膜上皮干细胞构建的工程化角膜上皮片,已成功用于治疗角膜缘干细胞缺乏症,部分患者恢复了角膜透明性和视力。
- 青光眼及视神经损伤:间充质干细胞因其神经营养和免疫调节特性,被探索用于保护视网膜神经节细胞、延缓视神经退行性病变。
该领域仍面临诸多挑战:细胞移植后的长期存活与功能整合效率有待提高;潜在的免疫反应(即便是自体细胞)和致瘤风险需长期监测;治疗成本高昂,产业化路径尚需优化;针对不同疾病阶段和亚型的个性化治疗方案仍需深入探索。
三、未来展望
干细胞治疗眼病的发展将呈现以下趋势:基因编辑技术与干细胞技术的结合,有望在移植前修正患者细胞的致病基因;3D生物打印或类器官技术可能实现更复杂眼组织结构(如多层视网膜)的体外重建与移植;人工智能将助力细胞质量监控与疗效预测。随着技术开发日趋完善、监管路径逐渐清晰,干细胞疗法有望在未来十年内成为部分目前无法治愈的眼病的标准治疗选择之一,最终实现从“延缓疾病”到“修复与再生”的根本性突破。
如若转载,请注明出处:http://www.yinmeisaier.com/product/8.html
更新时间:2026-04-20 20:59:34