厉害了,3D打印骨类器官!科学家开发出从干细胞到活体矿化骨神奇转变的新方法
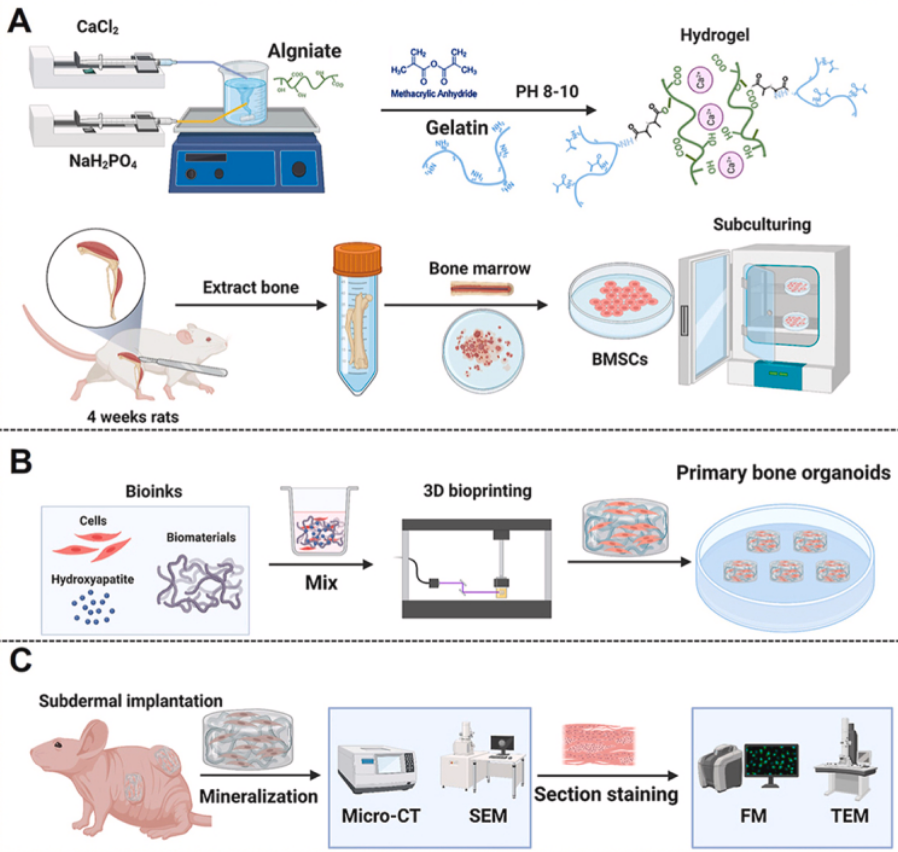
随着再生医学和生物材料科学的飞速发展,科学家们不断在组织工程领域取得突破性进展。其中,利用干细胞技术构建功能性组织替代物,尤其是针对复杂且再生能力有限的骨组织,一直是研究的热点与难点。一项发表于《生物活性材料》(Bioact Mater)的研究,报道了一种革命性的方法:通过先进的3D生物打印技术,成功引导干细胞经历一场神奇的“变身”,最终形成具有活体矿化结构的骨类器官。这一成果不仅为理解骨发育提供了新视角,更预示着未来个性化、功能性骨缺损修复的巨大潜力。
传统上,治疗严重骨缺损主要依赖自体骨移植或人工骨材料,但它们分别存在供区损伤、来源有限或生物活性不足、整合缓慢等问题。而干细胞,特别是间充质干细胞,因其强大的自我更新和多向分化潜能,被视为理想的“种子细胞”。如何在体外构建一个能精确模拟天然骨复杂微观结构(包括细胞排列、细胞外基质成分和力学特性)并促进干细胞高效、定向分化为成骨细胞的微环境,是技术上的核心挑战。
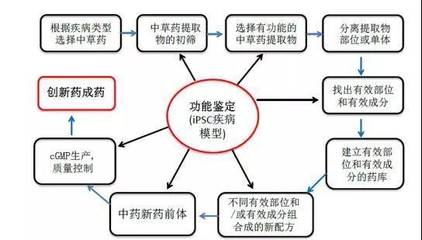
此次研究团队的创新之处在于,他们巧妙地将干细胞生物学与前沿的3D生物打印技术相结合。研究人员首先设计了一种特殊的生物墨水,这种墨水不仅包含作为支架的生物相容性高分子材料,更重要的是,它包裹着未分化的间充质干细胞以及一系列精确定制的生物活性因子和信号分子。这些成分共同构成了一个引导细胞命运的“程序化微环境”。
通过高精度的3D生物打印机,这种载有细胞的生物墨水被层层堆积,构建出预先设计好的三维结构,其形状和内部孔隙结构与目标骨组织高度仿生。打印完成后,这个结构并非静止不变。在体外特定的培养条件下,生物墨水中的信号程序被激活,开始精确地“指挥”干细胞的行为。干细胞在三维空间网络中接收连续的物理和化学信号刺激,逐渐启动成骨分化程序。
最令人惊叹的“神奇转变”随之发生:这些分化的细胞开始积极分泌骨特有的细胞外基质蛋白,如胶原蛋白,并在此基础上,高效地沉积羟基磷灰石等无机矿物成分——这一过程被称为“生物矿化”。随着时间的推移,最初的软质细胞-凝胶复合体,逐渐硬化、矿化,最终转变为一个具有机械强度、富含活细胞和天然骨矿物成分的“骨类器官”。它不再是简单的细胞团块或惰性支架,而是一个有生命、在结构和功能上高度模拟天然骨组织的迷你器官雏形。
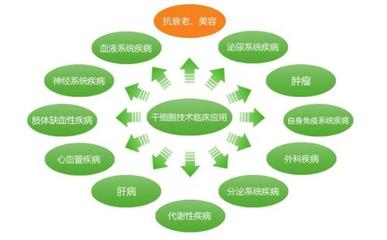
这项技术的意义非凡。它为研究人类骨骼发育、骨疾病机制以及药物筛选提供了一个前所未有的、高度仿生的体外模型。在临床转化方面,这种“活”的打印骨类器官具有极大优势:它来源于患者自身的干细胞,可避免免疫排斥;其形状可以个性化定制,完美匹配缺损区域;更重要的是,由于它在植入前已完成关键的分化与矿化,植入体内后能够更快地与宿主骨整合,加速愈合过程,有望实现大段骨缺损的功能性重建。
从实验室研究到广泛应用仍面临挑战,包括规模化生产、长期安全性验证、血管化集成以及监管审批等。但毋庸置疑,这项将干细胞技术与3D生物打印推向新高度的研究,标志着我们向按需制造活体组织与器官的宏伟目标迈出了坚实的一步。从干细胞到一块具有生命力的“骨头”,这场在培养皿中完成的魔法般转变,正在为无数受骨骼疾病困扰的患者带来新的曙光。
如若转载,请注明出处:http://www.yinmeisaier.com/product/5.html
更新时间:2026-04-20 06:28:09