CRISPR联手干细胞技术 Editas研发协议引领新一代细胞疗法开发
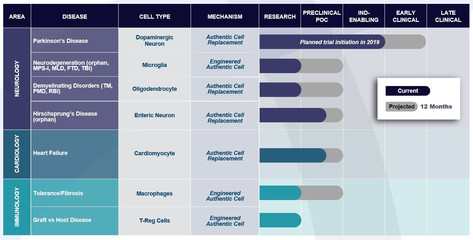
基因编辑领域的先驱之一Editas Medicine宣布达成一项重要的研发协议,其核心是将革命性的CRISPR基因编辑技术与前沿的干细胞技术相结合,共同开发下一代细胞疗法。这一战略合作标志着生物医药领域正朝着更精准、更高效、更具可扩展性的治疗模式迈进,为众多难治性疾病带来了新的曙光。
技术融合:当“基因剪刀”遇见“万能细胞”
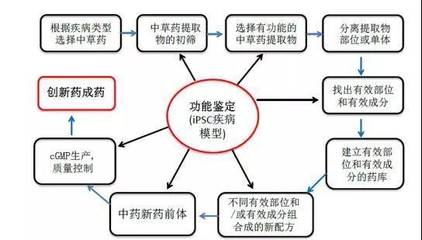
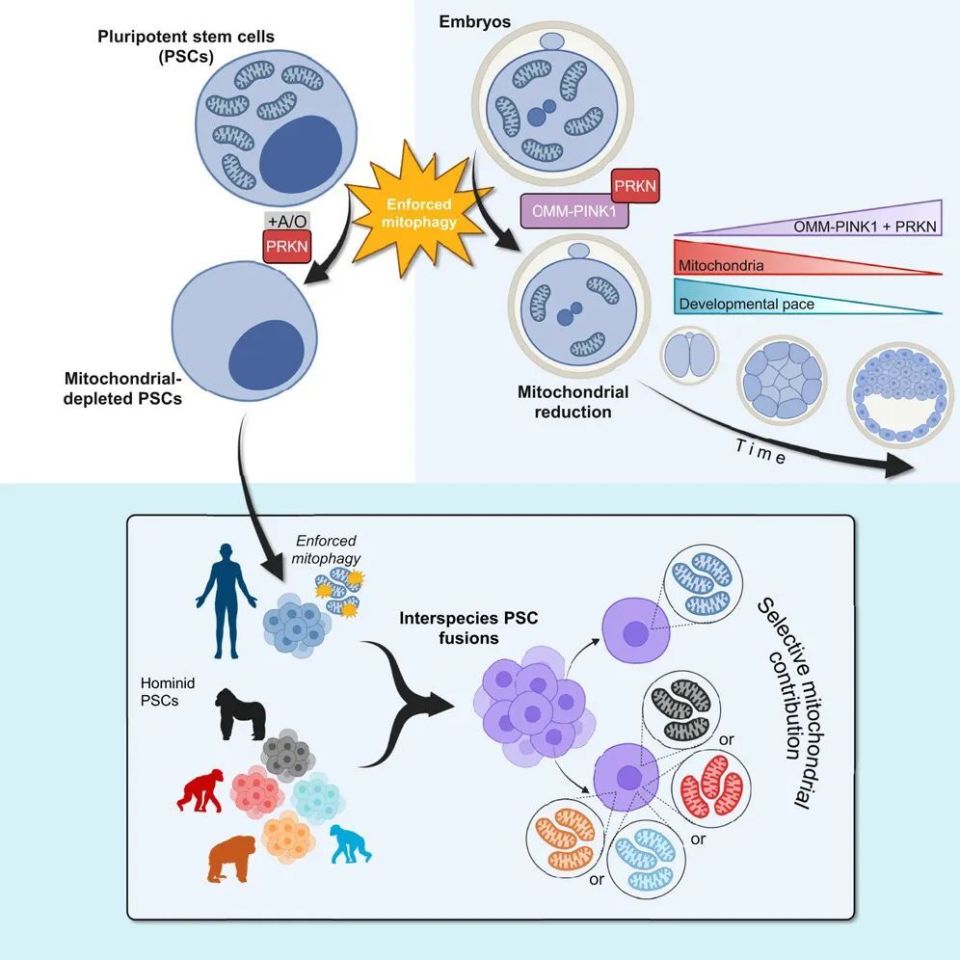
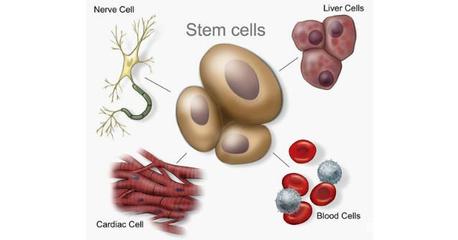
CRISPR-Cas9技术被誉为“基因剪刀”,能够以前所未有的精度对生物体的DNA序列进行定向编辑、修复或替换。而干细胞,尤其是诱导多能干细胞(iPSCs),因其具有自我更新和分化为多种功能细胞的“万能”潜力,被视为再生医学的基石。
此次合作的核心逻辑在于强强联合:
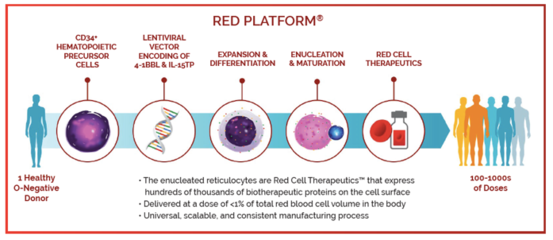
- 源头改造:在干细胞的“源头”阶段——即iPSCs或成体干细胞阶段——利用CRISPR技术进行精确的基因编辑。这可以用于纠正导致疾病的遗传缺陷(如镰状细胞病、某些遗传性眼病的致病突变),或者引入增强治疗功能的基因(如使免疫细胞能更好地识别和攻击癌细胞)。
- 规模化生产:编辑后的干细胞可以在体外大量扩增并定向分化为所需的治疗性细胞(如神经元、心肌细胞、胰岛β细胞或免疫细胞)。这解决了传统细胞疗法中细胞来源有限、个体化制备成本高昂的瓶颈,有望实现“现货型”通用细胞药物的规模化生产。
- 提升安全性与有效性:通过精准编辑,可以降低治疗细胞的免疫原性(减少排斥反应),增强其靶向性和持久性,同时避免非特异性编辑带来的潜在风险。
合作前景:聚焦疾病领域的突破
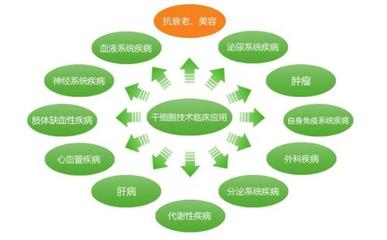
基于此项协议,Editas与合作方很可能会聚焦于几个关键疾病领域:
- 癌症治疗:开发通用型CAR-T或CAR-NK细胞疗法。通过编辑健康供体的干细胞,生成可大规模生产的、“即取即用”的免疫细胞,用于治疗多种血液癌和实体瘤。
- 遗传性疾病:针对由单基因突变引起的疾病,如遗传性视网膜疾病、血液疾病(β-地中海贫血)和某些神经系统疾病。在干细胞阶段修复基因后,将其分化为功能细胞并移植回患者体内。
- 退行性疾病与器官修复:为帕金森病(多巴胺神经元)、心脏病(心肌细胞)、糖尿病(胰岛细胞)等提供功能性的替代细胞来源。
行业影响与挑战
Editas此举并非孤例,它反映了整个生物技术行业的一个清晰趋势:将基因编辑、干细胞和细胞疗法进行深度整合。这种整合有望极大加速从实验室研究到临床应用的转化。
挑战依然存在:
- 技术挑战:确保基因编辑的绝对精准和高效,避免脱靶效应;控制干细胞分化为纯度高、功能完备的成熟细胞。
- 生产与监管挑战:建立符合药品生产质量管理规范(GMP)的、稳定的大规模生产工艺;面对这种新型复合疗法,监管机构需要制定相应的审评路径和安全标准。
- 临床验证:最终的安全性和有效性仍需通过严格的临床试验来证实。
Editas达成的这项研发协议,不仅仅是两家公司的技术联姻,更是为下一代细胞疗法绘制了一张充满希望的蓝图。它将基因编辑的“纠错”能力与干细胞的“再生”潜力融为一体,旨在从根源上治疗疾病。尽管前路仍有障碍需要克服,但这条技术路径无疑为无数患者带来了新的治疗可能,并持续推动着生物医学的边界向前拓展。干细胞技术开发,正因CRISPR的加入,步入一个更具操控性和想象力的新纪元。
如若转载,请注明出处:http://www.yinmeisaier.com/product/2.html
更新时间:2026-04-20 05:31:27